Der Drug Price Competition and Patent Term Restoration Act, auch Hatch-Waxman Act genannt, versucht, die Interessen von Markenarzneimitteln und Generika auszugleichen. Der erste Antragsteller für ein Generikum, dessen abgekürzter Antrag für ein neues Arzneimittel (ANDA) von der US-Arzneimittelbehörde (FDA) genehmigt wird, erhält ein 180-tägiges Marktexklusivitätsrecht. Der Exklusivitätsvorteil bietet einen großen wirtschaftlichen Vorteil für Generika, die als erste auf den Markt kommen. Das erste Generikum genießt das 180-tägige Marktexklusivitätsrecht in den USA, wobei die Marke einen bedeutenden Marktanteil erobert, bevor andere Generikahersteller auf den Markt kommen. Die große Mehrheit der in den USA verschriebenen Medikamente sind Generika. Es wird vermutet, dass einige Generikahersteller den größten Teil ihres Gewinns dadurch erzielen, dass sie als erste einen Antrag stellen und von der 180-tägigen Exklusivitätsfrist nach der Zulassung profitieren.
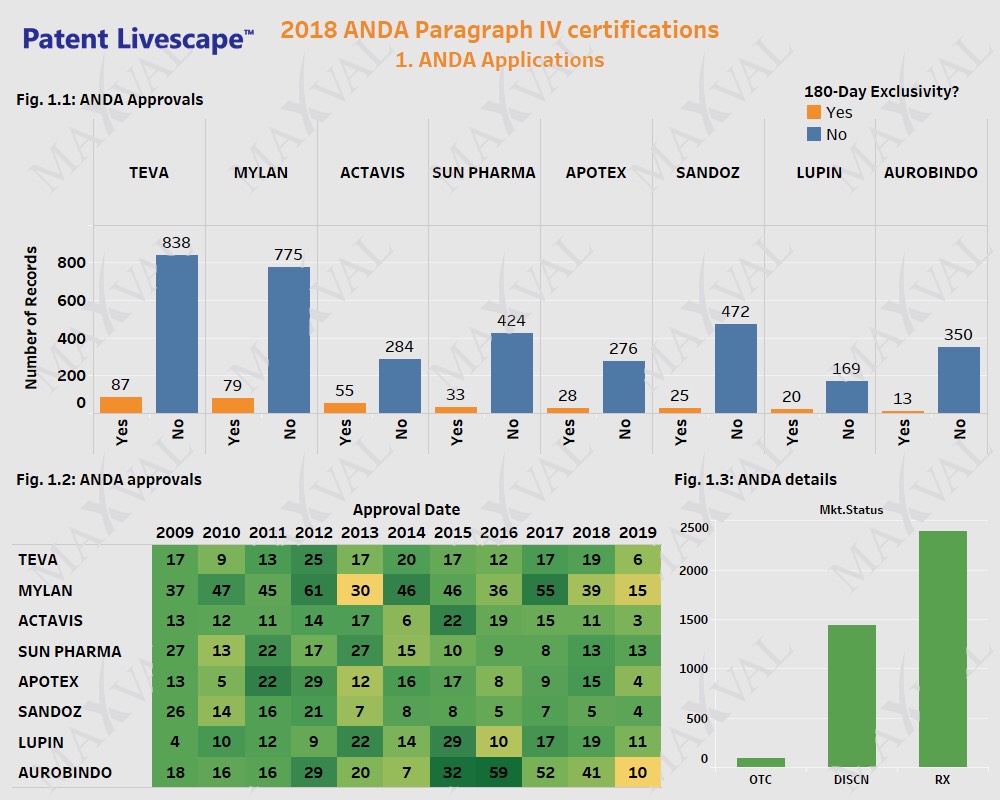
Etablierte Generikahersteller wie Teva, Sandoz, Apotex, Actavis, Sun Pharma, Lupin und Mylan versuchen schon seit langem, über ANDAs Marktexklusivität zu erlangen (Abb. 1.1). Mylan war unter den in den letzten 5 Jahren betrachteten Antragstellern am erfolgreichsten (Abb. 1.2). Mehr als die Hälfte der auf dem ANDA-Weg für die aufgeführten Unternehmen zugelassenen Arzneimittel befinden sich im aktiven Marktstatus und wurden überwiegend in Form von Tabletten oder Kapseln formuliert (Abb. 1.3).
Generikahersteller können die FDA-Zulassung für ihr Produkt noch vor dem Auslaufen des im Orange Book aufgeführten Patents erhalten, indem sie einen ANDA-Antrag mit einer Absatz-IV-Bescheinigung einreichen, die besagt, dass das aufgeführte Patent ungültig oder nicht durchsetzbar ist und/oder keine Verletzung vorliegt. Ein Paragraph-IV-Antrag bietet den finanziellen Anreiz für den Markteintritt von Generika. Der NDA-Inhaber wird vom ANDA-Antragsteller über die Absatz-IV-Bescheinigung informiert, die einen Rechtsstreit und eine 30-monatige Aussetzung des ANDA-Antrags auslösen kann.
Quelle: FDA
| Am 19. Juli 2019 genehmigte die FDA neun generische Versionen des Blockbuster-Medikaments LYRICA (Pregabalin) von Pfizer, das zur Behandlung von neuropathischen Schmerzen, Krampfanfällen und Fibromyalgie eingesetzt wird. Pfizer hatte den Markteintritt von Generikaherstellern für Pregabalin mit einem geschätzten weltweiten Umsatz von 5 Mrd. USD bisher erfolgreich verzögert. Zu den für die Freigabe von Pregabalin zugelassenen Generikaherstellern gehören Alembic Pharmaceuticals, Alkem Laboratories, Amneal Pharmaceuticals, Dr. Reddy's Laboratories, InvaGen Pharmaceuticals, MSN Laboratories Ltd, Rising Pharmaceuticals, Inc, Sciegen Pharmaceuticals Inc. und Teva Pharmaceuticals.
"Die heutige Zulassung der ersten Generika für Pregabalin, einem weit verbreiteten Medikament, ist ein weiteres Beispiel für das langjährige Engagement der FDA, den Zugang der Patienten zu kostengünstigen, qualitativ hochwertigen Generika zu fördern. Die FDA verlangt, dass Generika strenge wissenschaftliche und qualitative Standards erfüllen. Sichere und wirksame Generika effizient auf den Markt zu bringen, damit Patienten mehr Möglichkeiten zur Behandlung ihrer Krankheiten haben, hat für die FDA höchste Priorität." Dr. Janet Woodcock, Direktorin des FDA-Zentrums für Arzneimittelbewertung und -forschung |
Hier untersuchen wir die 2018 eingereichten Paragraphen IV-Anträge, gelistete Patente und Rechtsstreitigkeiten, um Einblicke in NDA-Strategien und bevorstehende Generikazulassungen zu erhalten.
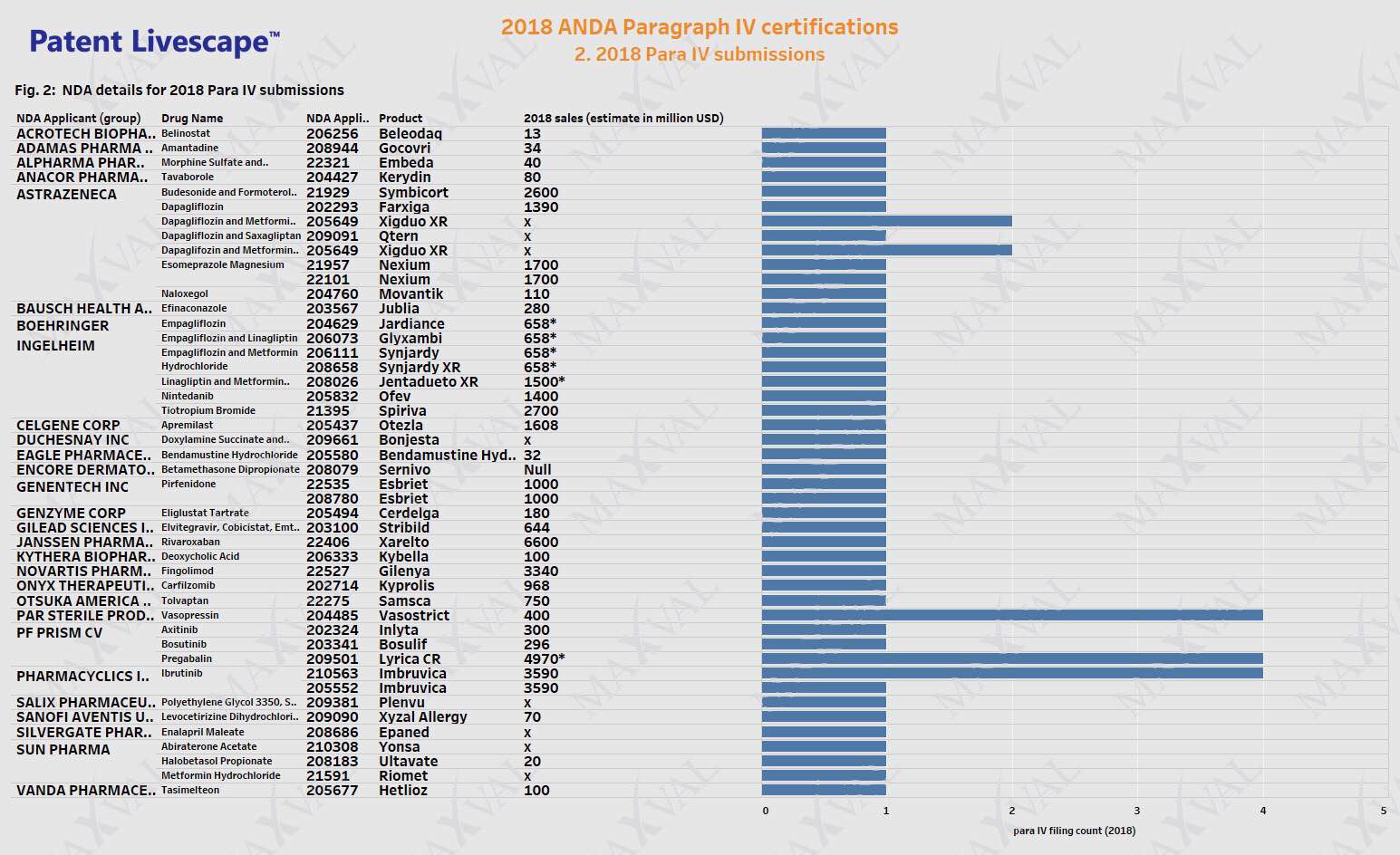
X, * - produktspezifische Verkäufe nicht verfügbar
Quelle: FDA
Die für das Jahr 2018 eingereichten Paragraph-IV-Anträge sind tabellarisch aufgeführt, wobei der Name des Arzneimittels, der Produktname, der Inhaber der NDA, der geschätzte Umsatz und die Anzahl der Anträge angegeben sind (Abb. 2).
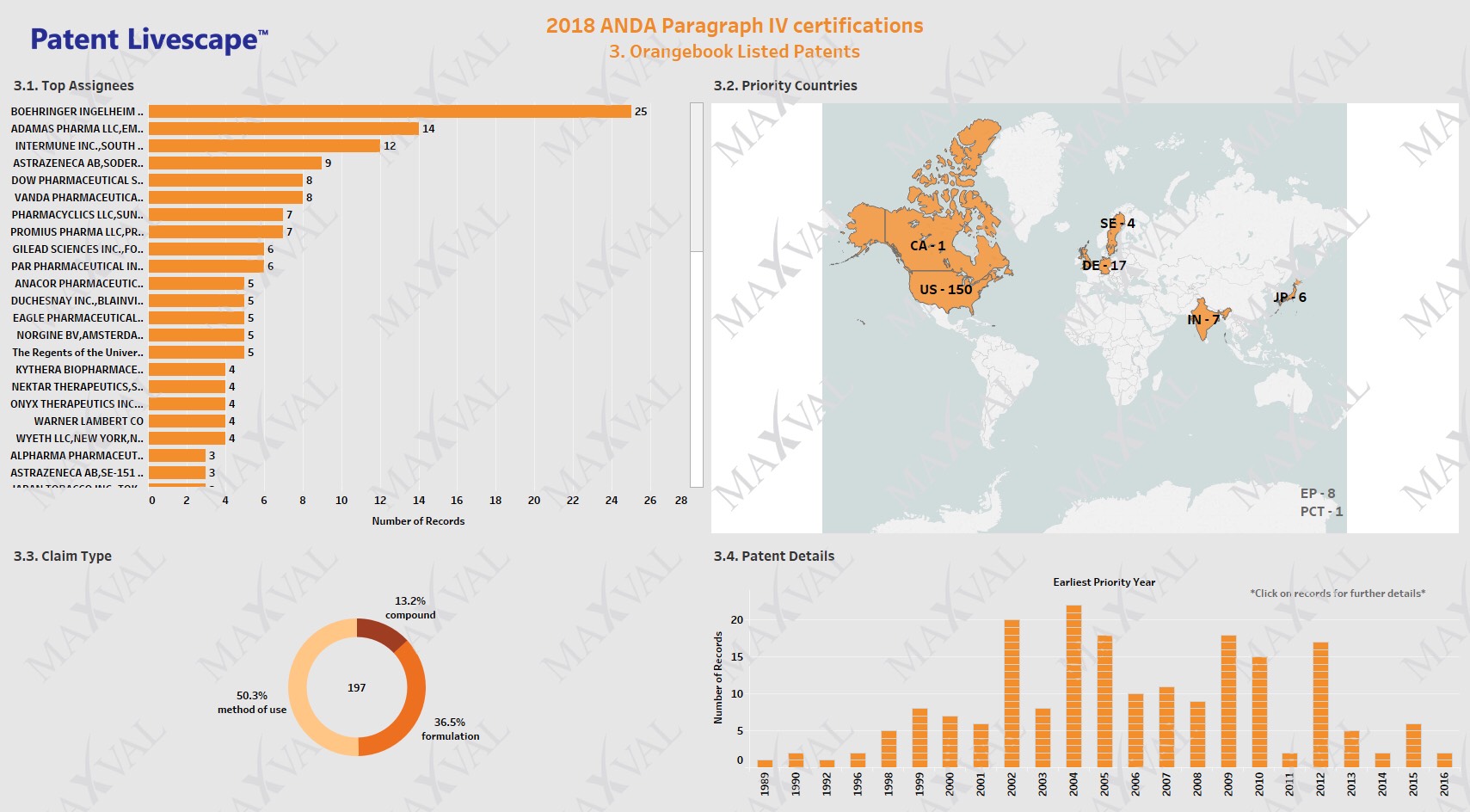
Wir analysierten die 197 im Orange Book aufgeführten Patente, die mit den Paragraph-IV-Anträgen und den damit verbundenen Rechtsstreitigkeiten zusammenhängen. Boehringer Ingelheim, Adamas Pharma, Intermune, Astrazeneca und Dow pharma waren die fünf wichtigsten Rechtsinhaber (Abb. 3.1). Die fünf wichtigsten Ursprungsländer für die verletzten Patente waren die USA, Deutschland, das EP, Indien und Japan (in dieser Reihenfolge). (Abb. 3.2). Unsere Analyse zeigt, dass sich mehr als 86 % der angefochtenen, im Orange Book aufgeführten Patente auf Verwendungs- oder Formulierungsmethoden bezogen und nur etwa 13 % auf Patente für pharmazeutische Wirkstoffe (API) (Abb. 3.3).
Quelle: FDA
Quelle: Litigation Databank
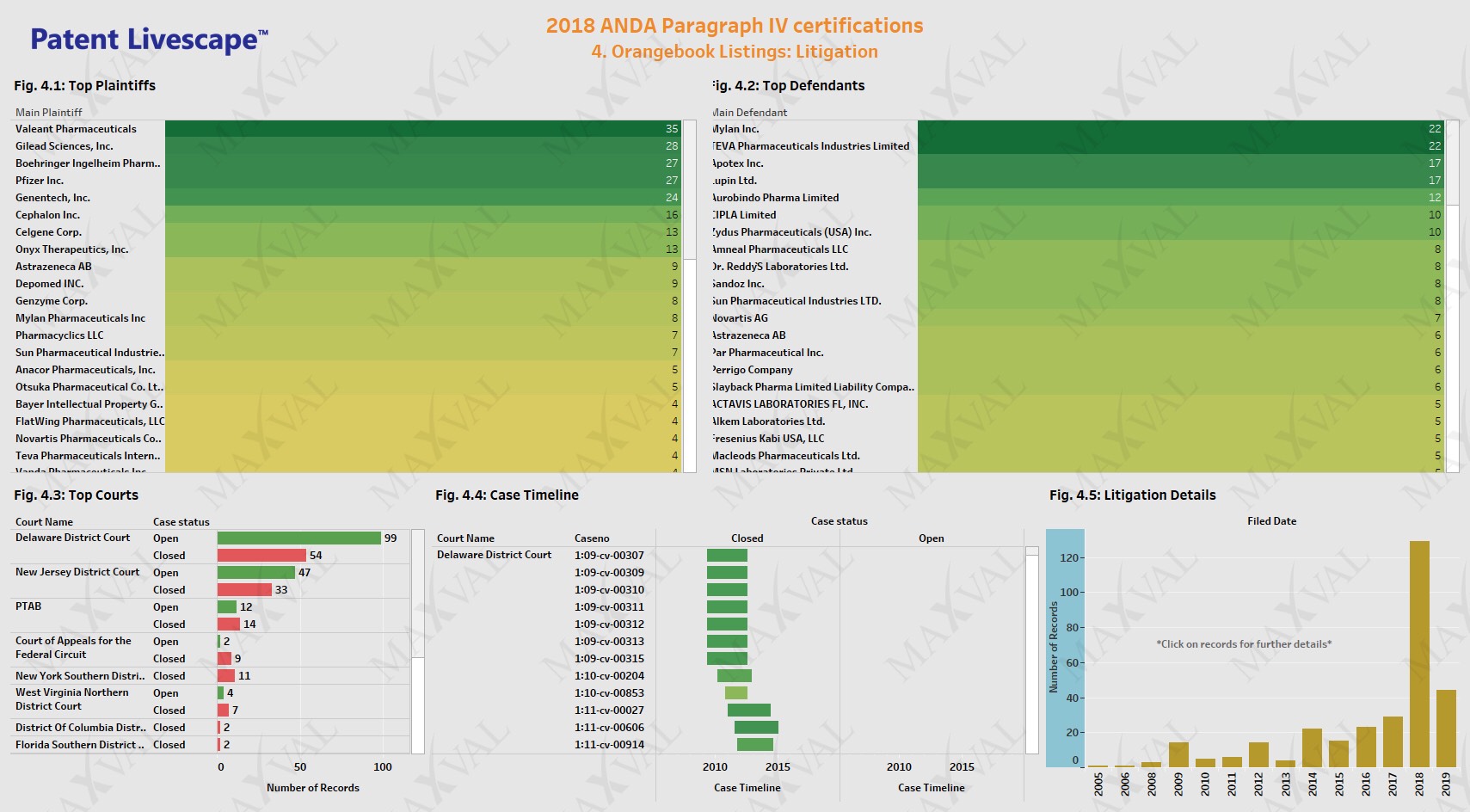
Als Nächstes untersuchten wir die US-Rechtsstreitigkeiten für die im Orange Book aufgelisteten Patente, die mit den Paragraf-IV-Anträgen in Verbindung stehen. Die 197 Patente wurden in 310 einzelnen Fällen angeführt. Die fünf Hauptkläger waren Valeant Pharmaceuticals, Gilead, Boehringer Ingelheim, Pfizer und Genentech (Abb. 4.1). Die 5 wichtigsten Beklagten waren Mylan, Teva, Apotex, Lupin und Aurobindo Pharma (Abb. 4.2). Fälle, die Pregabalin (LYRICA) und Axtinib (INLYTA) von Pfizer, die Kombination von Empagliflozin und Linagliptin (JARDIANCE, GLYXAMBI, TRADJENTA, JENTADUETO) von Boehringer Ingelheim und Eliglustat (CERDELGA) von Genzyme betreffen, Cobicistat (EVOTAZ, TYBOST) von Gilead, Dapagliflozin (FARXIGA) und Naloxegol-Oxalat (MOVANTIK) von Astrazeneca, Tolvaptan (SAMSCA) von Otsuka und Rivaroxaban (XARELTO) von Bayer beriefen sich auf Wirkstoffpatente. Für die Kläger waren die Bezirksgerichte in Delaware und New Jersey die erste Wahl, und die Fälle wurden überwiegend in den letzten zwei Jahren eingereicht (Abb. 4.3-4.5). Dies ist nicht überraschend, da die Richter in diesen Regionen über umfangreiche Erfahrung im Umgang mit ANDA-Streitfällen verfügen.
Die FDA hat im Jahr 2019 trotz eines Rückgangs im Juni 2019 über 900 ANDAs genehmigt. Die FDA hat kürzlich die Informationen zu den Paragraph-IV-Zertifizierungen und der Exklusivität für die Liste der Arzneimittel aktualisiert, für die ein oder mehrere im Wesentlichen vollständige ANDAs bei der FDA eingereicht wurden. Die aktuelle Liste der Paragraph-IV-Zertifizierungen enthält die Anzahl der eingereichten potenziellen ANDAs für den ersten Antragsteller, den Status der 180-Tage-Exklusivitätsentscheidungen, das Datum der Veröffentlichung der 180-Tage-Entscheidung, das Datum der ersten Zulassung des ANDAs für den "ersten Antragsteller", das Datum der ersten kommerziellen Vermarktung und das Ablaufdatum des letzten qualifizierenden Patents; sie enthält jedoch immer noch keine Angaben zum ANDA-Antragsteller für den anhängigen Paragraph IV. Es wird erwartet, dass die aktualisierten Paragraph-IV-Informationen den Generikaherstellern mehr Transparenz und Informationen über die in naher Zukunft eingereichten Paragraph-IV-Anträge und -Zulassungen sowie der Öffentlichkeit über die Verfügbarkeit kostengünstigerer Generika bieten.
Bleiben Sie auf dem Laufenden, wenn wir Sie in Zukunft über Generika und die Pharmaindustrie informieren. Die FDA-Zulassungen für Medizinprodukte gehen trotz der Herausforderungen durch COVID-19 weiter. Erfahren Sie, wie MaxVal Medizintechnikunternehmen beim Erwerb von geistigem Eigentum hilft.
Die Autoren: