Abbvie hat sich strategisch dagegen gewehrt, dass Konkurrenten ein Humira-Biosimilar in den USA einführen.
In seiner jüngsten Klage gegen Alvotech behauptet der isländische Biosimilar-Hersteller Abbvie, dass Alvotechs Biosimilar-Kandidat AVT02 Patente verletzt. In der am 28. Mai 2021 beim nördlichen Bezirksgericht von Illinois eingereichten Klage (1:21-cv-02899) wird behauptet, dass das Medikament von Alvotech gegen 58 Patente von Abbvie verstößt. Abbvie wird von Latham & Watkins und Finnegan, Henderson, Farabow, Garrett & Dunner vertreten. Die erste Klage von Abbvie war eine am 24. März 2021 am selben Ort eingereichte Klage wegen angeblichen Diebstahls von Geschäftsgeheimnissen durch einen ehemaligen Mitarbeiter von Alvotech. Abbvie hatte außerdem am 27. April 2021 am selben Ort eine Klage gegen Alvotech eingereicht (1:21-cv-02258), in der es um die Verletzung von vier seiner Patente ging.
Die jüngste Klage ist eine Reaktion auf die Klage von Alvotech USA vom 11. Mai 2021, die eine Feststellungsklage gegen Abbvie anstrebt. Dieser Fall ist derzeit vor dem Virginia Eastern District Court anhängig (2:21-cv-00265).
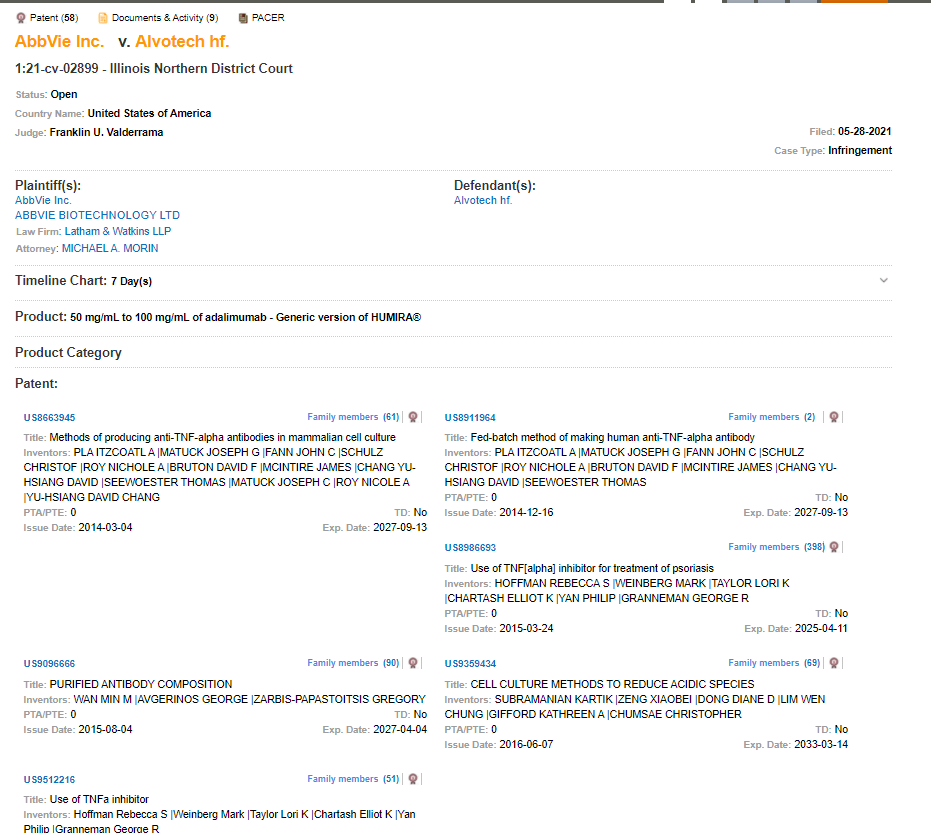
Quelle: MaxVal's Rechtsstreit-Datenbank
Humira hat sich in letzter Zeit immer wieder als das meistverkaufte Medikament erwiesen. Es wird erwartet, dass es in diesem Jahr einen Umsatz von mehr als 15 Milliarden Dollar erzielen wird. Das Medikament ist für die Behandlung mehrerer Entzündungskrankheiten zugelassen, darunter rheumatoide Arthritis und Morbus Crohn. Sein Wirkstoff, Adalimumab, ist ein vollständig humaner Antikörper, der auf den menschlichen Tumor-Nekrose-Faktor Alpha (TNF-α) abzielt.
Humira war in letzter Zeit das Ziel vieler Hersteller von Biosimilars. Auslöser für solche Biosimilar-Klagen ist ein bei der FDA eingereichter abgekürzter Lizenzantrag für Biologika (aBLA). Er wird durch den Biosimilar Price Competition and Innovation Act von 2009 (BPCIA") geregelt. Alvotech USA reichte seinen aBLA-Antrag zur Prüfung durch die FDA am 19. November 2020 ein. Der daraus resultierende "Patenttanz" zwischen Alvotech und Abbvie führte zum Austausch vertraulicher Informationen, darunter auch Patente von Abbvie. Alvotech wählte 4 der 62 von Abbvie identifizierten Patente für die erste Runde des Rechtsstreits aus. Abbvie hat die verbleibenden 58 Patente in der jüngsten Einreichung geltend gemacht.
Das vieldiskutierte Humira-Patentvermögen besteht aus mehr als 100 Patenten, die verschiedene Aspekte wie Behandlung, Verabreichung, Formulierung, Herstellungsverfahren und zugehörige Geräte abdecken. Es ist anzumerken, dass die Strategien von AbbVie zur Verlängerung des Lebenszyklus von Humira über Patentstreitigkeiten hinausgehen.
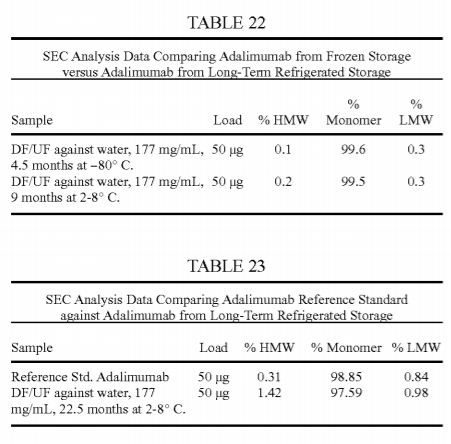
US9085619B2 mit dem Titel "Anti-TNF Antibody Formulations" und US8420081B2 mit dem Titel "Antibody Formulations and Methods of Making Same" beschreiben jeweils wässrige Formulierungen mit hoher Proteinkonzentration zur Herstellung von Antikörpern einschließlich Adalimumab.
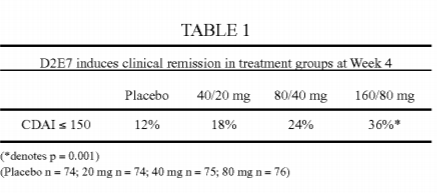
US8961973B2 mit dem Titel "Multiple-Variable Dose Regimen for Treating TNFα-Related Disorders" beschreibt ein Verfahren mit mehrfach variabler Dosis zur Herbeiführung einer klinischen Remission von Morbus Crohn. Dabei wird Adalimumab in Form einer ersten Induktionsdosis von 160 mg und einer zweiten Behandlungsdosis von 80 mg mit einem zweiwöchigen Abstand verabreicht.
US8926975B2 mit dem Titel "Method of Treating Ankylosing Spondylitis" (Verfahren zur Behandlung von Morbus Bechterew) beschreibt ein Verfahren zur Behandlung von Morbus Bechterew (AS), einer häufigen entzündlichen rheumatischen Erkrankung, die zu fortschreitender Steifheit der Wirbelsäule und Einschränkung der Beweglichkeit führt. Die Betroffenen sprechen möglicherweise nur unzureichend auf NSAIDs an. Die Patienten erhalten jede zweite Woche 40 mg eines isolierten menschlichen Anti-TNFα-Antikörpers, darunter Adalimumab.
| Unternehmen | Droge | FDA-Zulassungsdatum | U.S.-Einführungstermin |
| Amgen | Amjevita | Sep-2016 | Januar 2023 |
| Merck/Samsung Bioepis | Hadlima | Juli 2019 | Jun-2023 |
| Boehringer Ingelheim | Zyltezo | Aug-2017 | Jul-2023 |
| Mylan | Hulio | Jul-2020 | Jul-2023 |
| Novartis/Sandoz | Hyrimoz | Okt-2018 | Sep-2023 |
| Pfizer | Abrilada | November 2019 | November 2023 |
AVT02 von Alvotech ist eine hochkonzentrierte Adalimumab-Formulierung, die dem zitratfreien 100mg/ml-Produkt von Abbvie ähnelt. Es gibt weitere Adalimumab-Biosimilars mit niedrigerer Konzentration, die in den USA zum Verkauf zugelassen sind. Keines von ihnen wird jedoch aufgrund außergerichtlicher Einigungen vor 2023 auf den Markt kommen. So hat sich Amgen 2018 mit Abbvie geeinigt, wodurch sich der Markteintritt des Biosimilars in den USA bis 2023 verzögert. Alvotech rechnet mit einer FDA-Zulassung für AVT02 im vierten Quartal 2021. Es bleibt abzuwarten, ob Alvotech sein Biosimilar angesichts der Patentverletzungsklagen von Abbvie erfolgreich vor anderen auf den Markt bringen kann.
Laden Sie die vollständige Liste der von Abbvie geltend gemachten Patente hier herunter.